Enlace covalente
Tipos de enlace covalente
Existen dos tipos de sustancias covalentes:
Sustancias covalentes moleculares: los enlaces covalentes forman moléculas que tienen las siguientes propiedades:
- Temperaturas de fusión y ebullición bajas.
- En condiciones normales (25 °C aprox.) pueden ser sólidos, líquidos o gaseosas
- Son blandos en estado sólido.
- Son aislantes de corriente eléctrica y calor.
- Solubilidad: las moléculas polares son solubles en disolventes polares y las apolares son solubles en disolventes apolares (semejante disuelve a semejante).
Redes: además las sustancias covalentes forman redes, semejantes a los compuestos iónicos, que tienen estas propiedades:
- Elevadas temperaturas de fusión y ebullición.
- Son sólidos
- Son sustancias muy duras (excepto el grafito).
- Son aislantes (excepto el grafito).
- Son insolubles.
- Son neocloridas
simples: forma un electrón molecular ionizante.
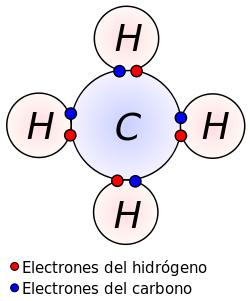
Un enlace covalente se produce por compartimiento de electrones entre dos o más átomos. Este tipo de enlace se produce cuando existe electronegatividad polar pero la diferencia de electronegatividades entre los átomos no es suficientemente grande como para que se efectúe transferencia de electrones. De esta forma, los dos átomos comparten uno o más pares electrónicos en un nuevo tipo de orbital, denominado orbital molecular. Losenlaces covalentes se suelen producir entre elementos gaseosos no metales.
A diferencia de lo que pasa en un enlace iónico, en donde se produce la transferencia deelectrones de un átomo a otro, en el enlace químico covalente, los electrones de enlace son compartidos por ambos átomos. En el enlace covalente, los dos átomos no metálicos comparten uno o más electrones, es decir se unen a través de sus electrones en el último orbital, el cual depende del número atómico en cuestión. Entre los dos átomos puede compartirse uno, dos o tres electrones, lo cual dará lugar a la formación de un enlace simple, doble o triple. En representación de Lewis estos enlaces pueden representarse por una pequeña línea entre los átomos
No hay comentarios:
Publicar un comentario